

생명과학과
면역치료, 세포치료제, 항체치료제, 암, 퇴행성 뇌질환실험실 : https://immunotherapylab.wpcomstaging.com/
교원 창업기업 : ㈜큐로셀(https://curocellbtx.com), ㈜일리미스 테라퓨틱스
연구내용
연구성과
□ In vivo 활성 조절이 가능한 Switchable CAR-T 플랫폼 개발
B 세포 항원인 CD19을 표적하는 CAR-T 세포는 급성 백혈병 환자에게서 높은 치료효과를 보였지만, 급격한 사이토카인 면역반응으로 인해 일부 환자가 죽음에 이르는 부작용이 보고되었습니다. 이는 기존의 약들이 투여량을 다르게 함으로써 독성에 대응하는 것이 가능한 것과는 다르게 세포 치료제가 환자에게 투여된 후 활성을 조절할 수 있는 방법이 없기 때문입니다. 이를 극복하기 위하여, CAR-T 세포의 활성을 조절할 수 있는 'switch' 분자를 도입하였습니다. 이 시스템에서 switchable CAR-T 세포는 switch의 tag 분자를 인식하여 이합체를 이루었을 때에만 비로소 표적 세포에 대한 활성을 유도할 수 있게 됩니다. 이러한 가설을 증명하기 위하여, FITC 소분자를 인식하는 CAR-T 세포를 제작하였고, 이와 함께 사용할 수 있는 FITC-접합 switch 항체를 제작하였습니다. 이후 세포주 및 xenograft 모델을 이용하여, 실제로 switchable CAR-T 세포의 in vivo 활성이 switch 항체 분자의 투여량에 따라 조절됨을 보였습니다. 또한 switch 투여량과 시기를 조절함으로써, 기존의 CAR-T 치료제가 보였던 급성 독성을 일으키지 않고도 암 xenograft 모델에서 완전관해를 유도할 수 있음을 보였습니다. 뿐만 아니라, switch의 생산 측면에서 수월성을 갖는 위해 효모의 전사인자인 GCN4 펩타이드 서열에 기반한 switchable CAR-T를 함께 개발하였습니다. Switchable CAR-T 플랫폼의 개발 및 전임상 실험결과를 바탕으로 해당 플랫폼은 다국적 제약기업인 Abbvie에 임상개발을 위해 기술이전 되었고, 현재 미국에서 임상 1상이 진행중입니다.
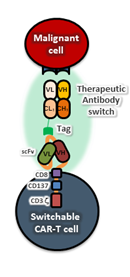
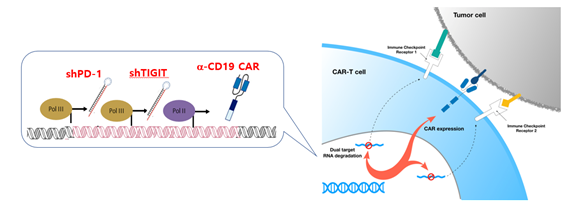
[Switchable CAR-T 접근법의 모식도] [PD-1과 TIGIT 2종의 면역관문 수용체가 억제된 CD19 표적 CAR-T 치료제 모식도]
□ 면역관문수용체의 발현이 억제된 Two-in-one CAR-T 플랫폼 개발
B 세포 항원인 CD19을 표적하는 CAR-T 세포는 급성 백혈병환자에게서 높은 치료효과를 보였지만, 만성 백혈병 또는 림프종 환자에게서는 상대적으로 낮은 반응률을 보임. 뿐만 아니라 고형암에서 CAR-T 치료제가 유의미한 치료 효과를 보인 예는 아직 보고된 바 없습니다. 특히, 실제 암환자의 90% 이상을 고형암 환자가 차지하는 상황에서, CAR-T 치료제의 치료영역을 고형암으로 확장하는 것은 시급히 해결해야할 매우 중요한 과제입니다. 고형암에서 CAR-T 치료제가 효능을 보이지 못하는 이유로는 암세포의 이질성, 면역억제환경, 또는 CAR-T 세포의 투과를 막는 물리적 장벽 등이 거론되고 있습니다. 특히 암세포 혹은 주변 면역세포들에서 발현하는 PDL-1과 같은 면역관문 리간드는 활성화 혹은 소진된 T 세포의 기능을 억제하므로, CAR-T 세포의 기능에도 악영향을 미치게됩니다. 이를 극복하기 위한 방법으로, 면역관문 차단항체와 CAR-T 세포의 병용치료가 시도되고 있으나, 독성 및 지나치게 높은 치료 가격의 문제를 갖고 있습니다. 따라서, CAR 벡터를 이용하여, CAR의 발현과 동시에 면역관문의 발현을 억제하는 short hairpin RNA를 발현하게되면 이러한 우려를 해소할 수 있을 것입니다. 실제로 이러한 two-in-one 벡터 시스템을 사용하여 제작된 CAR-T 세포에서 PD-1의 발현이 억제됨을 확인하였고 PDL-1을 과발현하는 in vivo xenograft 모델에서 기존의 CAR-T에 비해 향상된 항암효능을 검증하였습니다. 현재 임상에서 사용되고 있는 2종의 CAR-T에서 PD-1 수용체의 발현을 비교하였을때 CD28 보조자극 수용체가 41BB 보조자극 수용체에 비해 기본적으로 PD-1의 발현이 높음을 발견하였고, 이러한 차이가 NFAT 전사인자의 활성 세기 차이임을 규명하였습니다. 이러한 결과를 바탕으로 CAR의 구조와 PD-1 수용체의 발현이 각기 다른 CAR-T 세포들이 in vivo에서 보이는 항암 효능의 차이를 확인하였음. 뿐만아니라, PD-1의 발현이 세포 내재적으로 억제된 CAR-T의 경우 기존의 CAR-T에 비해 초기 활성화는 지연된 반면 장기적인 증식 및 항암 효능이 우수함을 보였습니다. T 세포의 기능을 저해시키는 면역관문 수용체는 PD-1말고도 여러 종류가 존재하는데, 우리 실험실에서는 다른 여러 종류의 조합을 테스트한 결과, PD-1과 TIGIT이라고 하는 두 종류의 면역관문 수용체를 억제하였을 때 독특한 시너지가 발생함을 발견하였습니다. 이를 바탕으로 ㈜ 큐로셀에서는 2종의 면역관문 수용체가 억제된 CD19-표적 CAR-T 치료제를 개발하였고, 전임상 연구를 완료하였습니다. 현재 이 CAR-T 치료제는 국내에서는 최초로 환자를 대상으로 CAR-T 임상 시험 단계에 진입하였습니다.
