

Bio and Brain Engineering
치료용 바이오소재 공학 연구실교원 창업기업 : ㈜엑소퍼트 (https://www.exopert.com, 공동창업), ㈜드노보바이오테라퓨틱스 (http://www.denovobio.co.kr/en/index.php, 공동창업)
연구내용
연구성과
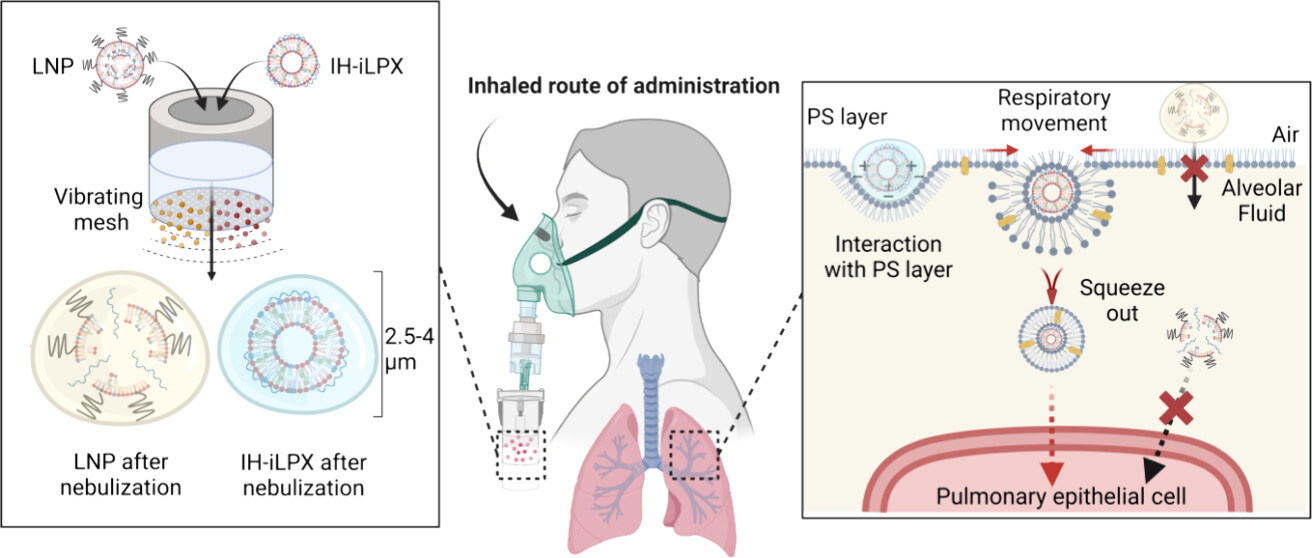
폐에서 자주 발생하는 감염성 및 난치성 질환을 mRNA 기반으로 치료하기 위해서는 폐에 mRNA를 효율적으로 전달하는 것이 핵심입니다. 네블라이저를 이용한 흡입이 mRNA를 폐에 전달하는 가장 유망한 방법으로 여겨지기 때문에, mRNA 흡입 전달을 위해 기존 mRNA 백신에 사용된 지질 나노입자를 활용하려는 많은 시도가 이루어졌습니다. 그러나 지질 나노입자는 전신 mRNA 전달이나 근육 내 백신 접종에 효과적임에도 불구하고, 네블라이징 과정에서 구조적 불안정성과 폐의 미세환경에 적응하지 못하는 한계로 인해 폐 전달에는 효과적이지 않습니다. 이러한 문제를 해결하기 위해서, 본 연구에서는 이온화 가능한 리포좀-mRNA 리포복합체를 개발했습니다. 이러한 리포복합체는 고도로 정렬된 지질 이중층 구조를 가져 네블라이징 시 안정성을 높이고, 폴리에틸렌 글리콜이 없는 조성 덕분에 낮은 혈청 환경과 폐의 계면활성제 층을 침투할 수 있습니다. 우리는 흡입된 나노입자의 폐 전달 과정을 모방한 다단계 스크리닝 절차를 통해 흡입에 최적화된 리포좀-mRNA 리포복합체를 찾았습니다. 이렇게 최적화된 리포복합체는 흡입 후 기존 지질 나노입자보다 높은 폐 내 형질전환 효율을 보였으며, 생체 내에서 독성도 관찰되지 않았습니다. 또한 폐 분포 분석 결과, 폐 깊은 곳에서도 균일한 단백질 발현이 나타났고, 상피 세포에 효과적으로 전달되었습니다. 이러한 연구 결과는 흡입형 mRNA 폐 치료제 개발에 관련된 도전 과제와 해결 방안을 제공하는 중요한 통찰을 제시합니다.
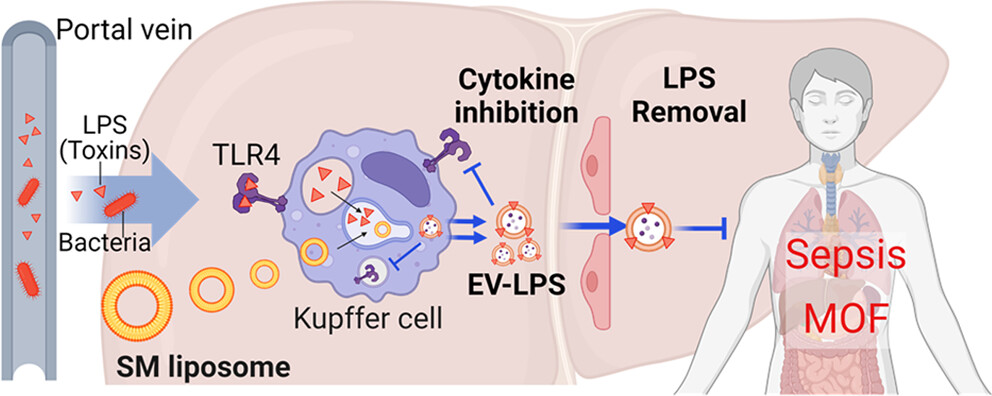
폐혈증은 여전히 전 세계 주요 사망 원인 중 하나이며, 치료 옵션이 제한적입니다. 지질다당류와 같은 독소를 표적으로 하는 항독성 전략은 전임상 연구에서 가능성을 보여 차세대 치료법으로 떠오르고 있습니다. 본 연구에서는 지질다당류 유도 패혈증에서 스핑고마이엘린 리포좀이 염증 반응을 조절하고 질병 진행을 억제하는 효능을 제시하였습니다. 우리의 연구 결과에 따르면, 스핑고마이엘린 리포좀이 지질다당류에 노출된 대식세포에서 세포외소포체 분비를 촉진하여 지질다당류의 세포외 방출 작용을 유도하였습니다. 또한, 스핑고마이엘린 리포좀은 세포외소포체 매개 지질다당류 외포작용을 통해 지질다당류에 의해 활성화된 대식세포에서 염증성 사이토카인의 생성을 감소시킵니다. 지질다당류 유도 패혈증 마우스 모델에서 스핑고마이엘린 리포좀의 전신 투여가 국소 및 전신 염증을 유의하게 감소시키고, 생존율을 향상시킴을 확인하였습니다. 이러한 결과는 스핑고마이엘린 리포좀이 세균 감염과 패혈증 치료를 위한 항독성제로서 잠재력을 지니고 있음을 보여줍니다.
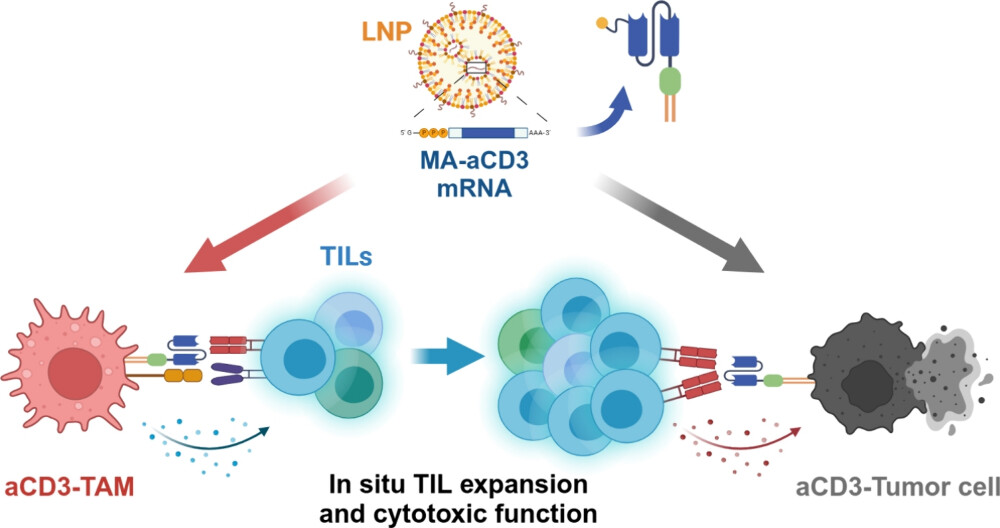
종양침윤림프구 요법은 진행성 흑색종과 전이성 대장암과 같은 공격적인 종양에 대한 임상 시험에서 유망한 반응을 보여주었습니다. 그러나 종양침윤림프구 요법은 복잡한 시험관 내 세포 준비 과정으로 인해 임상 적용에 여전히 제한이 있습니다. 본 연구에서는 고형암 치료를 위한 "자체(in situ) 종양침윤림프구 요법"을 제안합니다. 세포막에 고정되는 항-CD3 단일사슬항체조각(scFv)을 인코딩하는 mRNA를 전달하기 위해 지질 나노입자를 활용했으며, 이를 통해 종양 관련 대식세포와 종양세포 모두를 효율적으로 조작했습니다. 세포막에 고정되는 항-CD3 단일사슬항체조각의 발현은 종양 미세환경 내에서 종양침윤림프구의 활성화, 증식 및 종양세포와의 결합을 촉진했습니다. 흑색종 및 대장암 마우스 모델에서, mRNA 전달을 통해 종양 관련 대식세포와 종양세포의 막에서 항-CD3 단일사슬항체조각이 동시에 발현됨으로써 그 주변에 있는 다클론 CD8+ 종양침윤림프구의 증식과 종양세포에 대한 독성 효과가 발생해 유의미한 항암 효과를 나타냈습니다. 또한, 세포막에 고정되는 항-CD3 단일사슬항체조각 인코딩 mRNA와 PD-1에 대한 항체의 병용 치료는 PD-1 항체 치료에 대한 저항성을 가진 마우스 흑색종 종양에서 시너지적인 항암 효과를 보였습니다. 종합적으로, 본 연구 결과는 자체(in situ) 종양침윤림프구 요법이 고형암 치료를 위한 실용적이고 효과적인 mRNA 기반 치료법임을 시사합니다.
